【有機フッ素化合物の合成化学】
水素に次ぐファンデルワールス半径を有するフッ素は、全元素中最大の電気陰性度を示すとともに負電荷を持った酸素原子と等電子的です。こうしたフッ素の特性が有機フッ素化合物としての撥水性、脂溶性、耐熱性、あるいは安定性に大きく寄与しています。たとえばフルオロオレフィンはアミド結合と立体的・電子的に類似していてペプチド等価体としての利用などが検討されています。また、π電子共役系に摂動を与え、その電子構造を劇的に変化させる働きを示すこともあります。p型トランジスタ材料にペルフルオロアルキル基やp-トリフルオロメチルフェニル基を導入すると、フッ素を含まない有機材料を凌ぐ良好なn型トランジスタ特性が発現する研究を例として挙げることができます。したがって、フッ素を分子中の特定の位置に特定の立体化学で含む有機化合物を合成する新手法の開発は、特異な生理活性や優れた材料特性を発現する機能性有機分子の創製に必要不可欠なものです。
文献:M. Shimizu, T. Hiyama, Angew. Chem. Int. Ed. 2005, 44, 214-231.
トリフルオロメチル基置換リチオオキシランの立体選択的調製と反応
リチオオキシランは、オキシラニル基を有機分子へ求核的に導入できる有用な反応剤です。われわれは、ジクロロトリフルオロアセトン1のグリニャール付加により得られるジクロロヒドリン2を3当量の有機リチウム化合物で処理すると、リチウムとトリフルオロメチル基がシスに配置したリチオオキシラン3が効率よく発生することを見つけました。フッ素を含まないβ−オキシドカルベノイドは転位反応を起こしてカルボニル化合物を生じることが知られているので、この反応はフッ素があるからこそ起こる反応ということができます。また、リチオオキシランは通常オキシランの水素引き抜きで調製しますが、ここでは鎖状前駆体から置換基R2の導入を伴って立体選択的にリチオオキシランを発生させている点が先例のない特徴です。発生したリチオオキシラン3は、求電子剤で捕捉すればトリフルオロメチル基を含む四置換オキシラン4に、有機ホウ素化合物で処理するとトリフルオロメチル基を含む四置換オレフィン6に導くことができるので、トリフルオロメチル基を含む有機分子の合成反応剤としてたいへん有用です。また、この方法で合成した4のうち、置換基R1、R2がいずれもアルケニル基であるものについては、加熱するとコープ転位が速やかに進行して、対応するトリフルオロメチル基が2位に置換したジヒドロオキセピン5へと高収率で変換することができます。一方、3をジボロンで処理するとβ−トリフルオロメチルアルケニルボラン7を与えます。これにパラジウム触媒を使ってヨウ化アリールをカップリングさせると、トリフルオロメチル基置換トリアリールエテン8の立体選択的合成が可能です。この手法を使って、乳ガンの治療薬であるタモキシフェンのフッ素アナログとして開発されたパノミフェンの効率合成を達成しています。
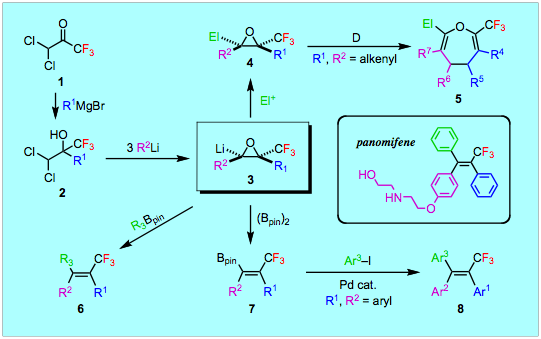
文献:J. Am. Chem. Soc. 2001, 123, 6947-6948; Tetrahedron 2003, 59, 9811-9823; Chem. Lett. 2004, 33, 438-439; Angew. Chem., Int. Ed. 2004, 43, 879-882; Heterocycles 2008, 76, 329-351.
トリフルオロメチル基置換トリアリールエテンの立体選択的合成:1,1-ジブロモ-2-トシルオキシ-3,3,3-
トリフルオロプロペンの立体選択的交差カップリング反応
トリフルオロメチル基を含む多置換アルケンを立体選択的に合成する新手法として、市販の1,1-ジブロモ-3,3,3-トリフルオロアセトンから一工程で得られるエノールトシラート1が脱離基の三つ置換したトリフルオロプロペンと見なせることに着目し、これに有機ホウ素反応剤とのカップリング反応を3回繰り返して、トリフルオロメチル基置換トリアリールエテン4を自在に合成することに成功しました。すなわち、1の1段階目の交差カップリングがトリフルオロメチル基のシス位で立体選択的に進行すること、高いシス選択性の発現にはフッ素の存在が必須であることを明らかにしています。この成果は、脱離基が三つ置換したエテン誘導体のカップリング反応を基盤とする四置換エテンの立体選択的合成の最初の例です。この手法を用いると、作用させるホウ素反応剤の順序を変えるだけで、任意の立体異性体を選択的に合成することができます。上述の研究がトリフルオロメチル基を含む有機金属反応剤の開発と反応を主体としているのに対し、ここではトリフルオロメチル基を含む多官能性求電子剤の創製と活用が研究の主眼となっています。
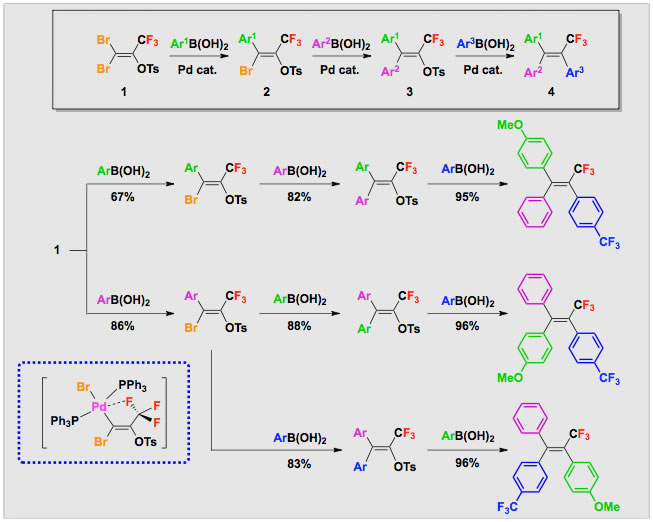
文献:Angew. Chem. Int. Ed. 2007, 46, 8659-8661; Bull. Chem. Soc. Jpn. 2011, 84, 1339-1341.
トリフルオロプロピニルリチウムを軸とする有機フッ素化合物の簡便合成
炭素―炭素三重結合が様々な化学変換をおこなえるため、トリフルオロプロピニル基を有する化合物は、トリフルオロメチル基置換生物活性化合物や機能材料合成のための有用なC3合成ブロックになると考えられます。この観点にたってわれわれは、入手容易な1,1,-ジクロロ-3,3,3-トリフルオロ-2-トシルオキシプロペンからトリフルオロプロピニルリチウムを簡便かつ定量的に調製できる方法を開発しました。そして、トリフルオロプロピニルリチウムをカルボニル付加して得られるプロパルギルアルコールをスルホニル化したあと、有機亜鉛反応剤とカップリングすると、これまで合成法がほとんど開発されていないトリフルオロメチル基を含む三および四置換アレンが簡便に合成できることも明らかにしました。また、トリフルオロプロピニルリチウムトリフルオロプロピニルリチウムをトリメトキシボランで捕捉してKHF2で処理すると、対応するボラート反応剤を調製することができます。一方、トリフルオロプロピニルリチウムに塩化トリブチルスズを作用させて調製したトリフルオロプロピニルスズは、パラジウム触媒を用いるとアルキンに位置および立体選択的にカルボスタニル化することを見つけました。フッ素の存在がカルボスタニル化反応の促進に寄与していることもわかっています。この反応はトリフルオロメチル基置換エンインの立体選択的合成法として有用です。
さらに、トリフルオロプロピニルスズにPhI(CN)OTfを低温で作用させ、単離操作を工夫することによってこれまで報告のなかったトリフルオロプロピニルヨードニウム塩の合成に初めて成功しています。そして、このヨードニウム塩がディールズアルダー反応のジエノフィルとして高い反応性を示すことを見つけ、トリフルオロメチル基置換シクロヘキセン誘導体の簡便合成法を確立しました。
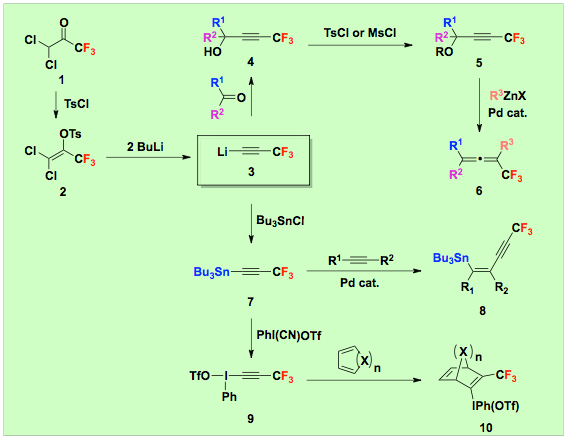
文献:Chem. Lett. 2005, 34, 1700-1701; Synlett 2007, 1163-1165; Chem. Lett. 2008, 37, 1304-1305; Future Med. Chem. 2009, 1, 921-945.
含フッ素カルベノイドの創製とモノおよびジフルオロ化合物合成への展開
ポリハロメチルリチウムは高い求核性を有すると同時に、これを求電子剤で捕捉して得られる生成物にはさらなる官能基変換や炭素−炭素結合生成の手がかりとなるハロゲンが存在するので、有機合成上有用な増炭剤です。したがって、フルオロポリハロメチルリチウムは有機分子にフッ素原子を一つ導入する優れた反応剤として期待できますが、フッ素の孤立電子対の影響で非常に分解しやすい性質を持っています。われわれは、カルボニル化合物存在下トリブロモフルオロメタン (1) に –130 °Cでブチルリチウムを作用させると、生じる含フッ素カルベノイド2が速やかに反応して、対応する付加体3を良好な収率で与えることを明らかにしました。付加体3は、残る臭素や水酸基を手がかりにして、peptide isostereとして注目を集めるフルオロオレフィンやジフルオロオレフィンなどに導くことができます。
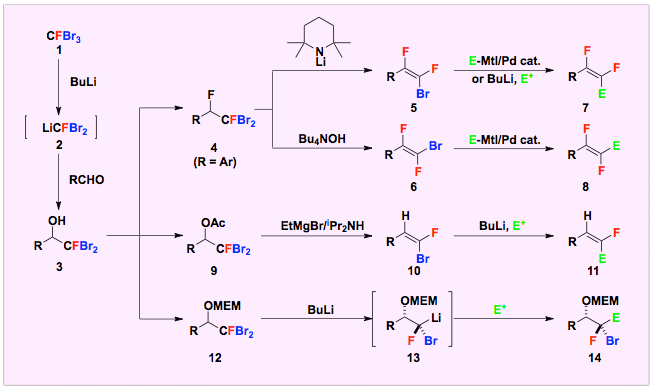
文献:Synlett 1996, 831-832; Tetrahedron Lett. 1996, 37, 7387-7390; Bull. Chem. Soc., Jpn 1998, 71, 2903-2921; Bull. Chem. Soc. Jpn. 2000, 73, 1691-1695.
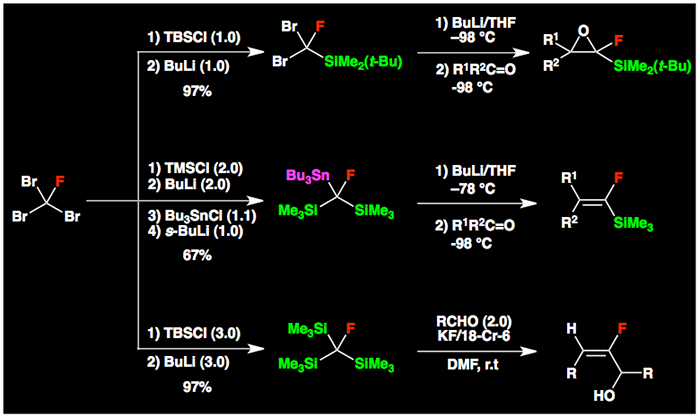
また、トリブロモフルオロメタンの臭素を一つ、二つあるいは三つともシリル基で置換すると、熱的安定性の向上したモノフルオロメチルアニオンを発生させることができることを見つけています。これらのアニオン種をカルボニル付加させると、置換するシリル基の数に応じて、フルオロオキシラン、フルオロオレフィンあるいはフルオロアリルアルコールを作り分けることができます。
文献:Tetrahedron Lett. 1997, 38, 4591-4594;Tetrahedron Lett. 1999, 40, 7375-7378; Heterocycles 2000, 52, 707-717; Bull. Chem. Soc. Jpn. 2000, 73, 1685-1690.